2019年にESCより発表されたガイドラインでINOCAという言葉が掲載された。近年冠微小血管障害(CMD)の評価が大変注目されてきている。そこで今回、CMD評価の経験豊富な先生方から、その測定意義と評価におけるexperienceを学んでいく。
横井宏佳先生(福岡山王病院)、園田信成先生(佐賀大学)

INOCA総論〜CMDを理解する〜
水上拓也 先生(昭和大学)

CMDとは、病態生理医学的には微小な冠動脈の障害を有している状態を指す。つまり、前細動脈、細動脈に障害があり、以降の動脈に血流が十分に供給されず心筋虚血を起こしている状態である。この概念は古くから微小血管狭心症(MVA)という概念で存在し、以前はシンドロームXといわれ、狭心症状があるにもかかわらず冠動脈造影所見では正常である病態として総称されていた(図1)。
INOCA症例における、CFR・IMRを用いて評価するCMDを紹介する。INOCAはIschemia with NoObstructive oronary Artery Disease の略で、INOCAのエンドタイプは、MVAと冠攣縮性狭心症(VSA)の二つに分かれる(図2)。具体的にはMVAの病態生理学的な分類がCMDであり、IMRもしくはCFRの異常があり、心外膜血管に狭窄のない患者が該当する。一方、VSAはIMR、CFRが正常でアセチルコリン負荷による陽性患者が該当する。このように、INOCAの予測因子はある程度分かっており、高血圧、糖尿病、喫煙、高齢などのファクターにおいて、INOCAの割合が多いといわれている。
INOCAの中でもCMDについて詳しくみていく。FFRが正常であり、IMRが高いとCMDが疑われるが、この場合、心外膜血管に狭窄が無いため、心臓に起因する狭心症ではないと判断されるかもしれない。実際メタ解析をした論文では、CMDを罹患している患者は約5倍のMACEリスクを持っており、死亡率においては約4倍と、CMD罹患患者の予後は悪い。治療法としては、栄養、運動、体重管理、禁煙、ストレス改善などの生活習慣の改善、さらにはリスク因子の管理、高血圧や脂質異常症、糖尿病管理などが重要となる。薬物治療は、CMDではβブロッカー、カルシウム拮抗薬、ニコランジルを用いる。VSAに対してはカルシウム拮抗薬、硝酸薬、ニコランジルが推奨されている。CMDの患者をアセチルコリン負荷とCFR、IMR測定で層別化し、治療を標準化することによる患者ベネフィットを評価したCorMicA Trialが2020年に報告された。その報告によると、アセチルコリンや微小血管評価で層別化した患者において、彼らの提唱する適切な薬物治療を行うことで6カ月後の狭心症の症状(SAQ) が改善されていた。しかし、INOCAに対する治療の検討はまだ不十分であり、今後の検討が必要である。
ではCMDはどのように評価するのか。非侵襲的なSPECTは、LAD領域、LCX領域、RCA領域における虚血評価はできるが、感度は低い。実際にPACIFIC研究でFFRをレファレンスにした場合、心外膜冠動脈の評価においてSPECTのAUCは0.70と、CT、PET、FFRctと比べて低かった。2019年のESCガイドラインではSPECTは推奨するCMD測定モダリティのリストにない。また、同ガイドラインでCMD評価に関する改訂があり、guidewire-basedのCFR・IMR測定の推奨レベルもクラスⅡBからクラスⅡAに上がっている。このようにESCガイドライン上においても侵襲的なCMD評価を加えることによって、患者にとってよりベネフィットのある治療選択、薬物治療を行うことが求められている。
以上をまとめる。
1. 心外膜血管が正常であっても、CMDを有する患者予後は良くない。
2. CMDに対する治療の報告はあるが、まだ確立はされておらず、今後の検討が必要である。
3. INOCAという概念に従った診断・治療でCMD患者の予後改善が期待できる。
4. CMDの診断には微小循環障害を定量化できるIMRがスタンダードになりつつある。
川瀬先生:IMRが高いときの治療方針について、臨床にて迷うケースが多いのですが、ヨーロッパでの判断基準や治療傾向など教えてください。
水上先生:IMRが高い場合でも、CMD合併、vasospasm合併など病態が複雑になっていますので、IMRのみで治療を決定できるのかというとまだ難しいと思います。アセチルコリン、もしくはエルゴノビン負荷試験とIMRを組み合わせた診断手法の報告もあり、病態に合わせた診断による適切な治療が可能になると期待しています。
齋藤先生:IMRのカットオフ値が正確には定まっていないですよね。CFRが低く、IMRが高い症例では微小循環障害があると考えて治療をしますが、CFRとIMRの乖離現象も多く経験します。
水上先生:IMRのカットオフ値は23~28を選択することが多いです。しかし、そこに手技の影響も少なからず影響してくると思いますので、今後、IMRの手技自体やソフトウエアの改善にも期待したいと思います。
横井:水上先生ありがとうございました。
INOCA症例に対する適正な診断とは
高橋 潤 先生(東北大学)

虚血性心疾患は、インターベンションの適応となる器質的冠動脈疾患、冠攣縮、そして冠微小血管障害の3つの成因から成る。冠動脈機能異常が関与する冠攣縮性狭心症と微小血管狭心症が非閉塞性冠動脈疾患(INOCA)の本態であると考えられている。INOCAの中でよく直面するのが心表面の攣縮、いわゆる冠攣縮であり、確立した診断法としてアセチルコリン負荷試験が挙げられ、感度90%、特異度99%と非常に診断精度の高い検査である(図3)。
冠攣縮が狭心症の機序であったINOCA症例を紹介する。60代の男性、朝方の安静時・労作時の胸部圧迫感を訴えて来院。運動負荷心電図を外来で施行したところ心電図においてSTが下がり胸部症状が出現し、明らかに虚血性変化を示した。狭心症が疑われたためカテーテル検査を実施したが有害狭窄が認められないため、カテーテル検査台の上でエルゴメーターを用いて運動負荷を行ったところ、胸痛発作と心電図変化が見られ、さらに冠動脈造影でも右冠動脈中部に99%高度狭窄が出現した。以上の所見から運動誘発性冠攣縮と診断した。冠攣縮性狭心症では安静時のみならず運動時にも胸部症状を認めるという報告は珍しくない、INOCAの診断においては、動脈硬化性変化に乏しく、有意狭窄が認められなくても思考停止せず患者の訴えや状況を聞いて同様の症状を冠攣縮誘発試験等により再現することが非常に重要である。INOCAが引き起こされる機序が明らかにされることにより適正な治療法、例えば冠攣縮を予防するカルシウム拮抗薬など適切な治療法を選択することができる。
そもそも冠微小血管は非常に繊細にコントロールされており、冠血流の自動調節能を担っている。これが微小血管攣縮や、拡張能異常により、心筋酸素需要量を確保できなくなり心筋虚血が引き起こされる。このような背景から、微小血管の評価を含めた包括的冠動脈機能評価としてInterventional Diagnostic Procedures(IDP)の概念が近年ヨーロッパで提唱されるようになった。
IDPは以下の3段階から成り立つ。
ステップ1:器質的評価(冠動脈造影)
ステップ2:冠動脈収縮反応評価(アセチルコリン負荷試験)
ステップ3:微小循環評価(圧・温度センサー付きガイドワイヤーによる検査)
当院においてはアセチルコリン負荷試験を先行させているが、ヨーロッパではステップ3を先行させている施設もある。さらに当院では、アセチルコリン負荷試験を行うときに微小血管攣縮評価のため冠静脈洞(CS)にカテーテルを挿入して心筋乳酸産生を評価している。手順としては、アセチルコリンを20、50、100と左冠動脈に入れた後、造影で血管攣縮が起こっているか確認し、その後にCSと左冠動脈のカテーテルから採血をして、冠動脈入口部とCSの乳酸値を測定する。健常な場合、冠動脈入口部の乳酸値は高く、CSの乳酸値は心臓の中で消費され低くなる。ところが心筋内で虚血が起こると、この乳酸値が逆転し、虚血状態の最も鋭敏な指標の一つとして報告されている(図4)。さらにステップ3における当院における取組は、CFR・IMR測定の際、アデノシンによる最大充血後にIMRを測定し、さらにその後、Rhoキナーゼ阻害薬ファスジル冠注による最大充血後にもIMRを測定した。
次は、胸痛を訴えて来院するも冠動脈造影上狭窄がなかったため、INOCAを検討した症例でアセチルコリン負荷を実施したところ、20μgでは25%程度の狭小化であるが、100μgでは末梢で有意な狭窄が起こり冠攣縮性狭心症と診断した。さらに20μ負荷時の乳酸値を測定すると、逆転現象が確認されたため、この症例は冠攣縮性狭心症と微小血管狭心症の合併例だということが分かった。別の症例では、INOCA疑いの患者に対し、ステップ2で20μgでも100μgでも心表面の冠動脈攣縮はみられなかった。ところが100μg負荷時に心電図に虚血性の変化があり乳酸値の逆転が起こったため、この症例は単独の微小血管性の狭心症と診断した。IMR値は28.9と異常値であったが、Rhoキナーゼ阻害薬ファスジルを冠注した後に測定すると、IMRが13.9へ低下した。これは、Rhoキナーゼ活性が亢進しIMRを押し上げていたためであり、微小血管の拡張能低下を示唆するものである。当院では、187例でIDPを行い、心表面冠攣縮の有無とIMRの高低で4群に分けた場合、心表面に冠攣縮があり、微小血管抵抗が高い群では有意に予後が悪いということが分かった。特筆すべきはそこに共通のメカニズムとしてRhoキナーゼが関与していることであった。
最後にまとめると、INOCAにおいて冠動脈機能異常は虚血を引き起こす主な要因であり、その診断は患者の訴えに耳を傾けることからはじまる。IDPは可視化が不可能な冠微小血管を含め、包括的に冠動脈機能を評価することを可能とし、INOCA患者の予後予測や治療戦略の決定に有用であるといえ、われわれインターベンショナリストが今後さらに積極的に行っていくべきと考えられる。
園田先生:乳酸値と心電図変化の一致の精度はどう考えられますか?
高橋先生:基本的に、心電図変化があり、症状があるときには乳酸値が逆転する比率はかなり高いと思います。乳酸値が逆転して微小血管狭心症と診断した症例は、硝酸薬の冠動脈内投与後も虚血が持続していて、逆転したまま戻らないという症例も多く経験します。
嵐先生:微小循環の攣縮、あるいは微小循環障害に対して、ファスジルは臨床で使う薬ではないと思いますが、実際に同じような機序を持つ薬として実臨床ではどのような薬を使っていますか。
高橋先生:抗炎症作用があって血管拡張作用があるとなるとカルシウム拮抗薬ですね。ベニジピンかニフェジピンCRを第一選択として使用しております。その根拠としては抗炎症作用とRhoキナーゼ活性を抑えるというところです。
川瀬先生:日本においてはアセチルコリン負荷後の微小循環評価がメインになっているかと思われますが、その際に微小血管攣縮がまだ少し残っていてIMR値が高いと感じられるケースがあります。診断において何か気を付けることがございましたら教えて頂けますでしょうか?
高橋先生:アセチルコリン負荷後、最大拡張を図っても本当に最大拡張が達成されているかどうかについては、中々判断が難しいと思います。我々はファスジルという薬を投入しIMRの低下を確認しておりますが、アセチルコリン負荷後の完全拡張を確認し評価するという事は、今の技術ではまだ難しいかと思われます。
冠循環生理学的指標によるPost PCI Resultの評価
塩野泰紹 先生(和歌山県立医科大学)

CMDの中でPCIに関連するタイプ4の医原性にフォーカスをあてる(図5)。
症例を提示する。80歳代の女性で、高血圧、心筋梗塞の既往があり、胸部大動脈瘤や慢性腎臓病がある。下壁のMI後で、残枝のLADに対してPCIを行っている。前下行枝に石灰化を伴う高度狭窄があり、FFRは0.8を下回ったためPCIとなった。石灰化のためロータブレーターを行ったところ、スローフローにはならないものの、心電図にST上昇がみられ、典型的なPCIに伴うmicrovascular injuryと考えられた。
70歳代の男性で糖尿病と脂質異常症の既往歴がある。前下行枝の病変があり、RFRは0.87、FFRも0.78で虚血陽性の判定であった為、PCIを施行した。プレのIMRは15、CFRは2.9であった。#7〜6にかけてステントを留置し十分なフローが確保されていた。しかし、ステント留置後にFFR、RFRを測定したところ、RFRは0.87から改善がみられず、FFRは0.88と良好な改善が得られた。ポストFFRは0.92を上回ったほうが良いとする報告や、また、FFR0.88や0.86といった報告もあり最も低い報告では、0.84と報告がある。このようにステント留置後にFFRは改善するがRFRが改善しないことはある。IMRをみてみると28と上昇、CFRは1.8へ低下していた。IMR値から長いステントを脂質が多い病変に留置したことで、遠位塞栓により微小循環障害を起こしていると考えられた(図6)。
最後に、PCI後のMIは心不全の原因の一つとされており、それにより心血管イベントが起こるといわれている。IMR測定で血管造影や心電図よりも鋭敏にPCI後の心筋障害や心筋梗塞を同定できる可能性がある。

齋藤先生:PCI後の指標として、どれが優れていると思われますか。
塩野先生:まずPCI後に測定するのであればFFRだと思います。今回の症例のようにPCIにより安静時の血流が変化している可能性があるため、PCI後の指標としてはFFRが安定していると思います。RFRの良さはPCIの前に予測できるということなので、PCI前に測定するのであればRFRと考えます。
園田先生:一つ質問が来ています。中等度病変を有する患者にCMDが合併していた場合にFFRが偽高値になることはありますでしょうか。もしそうなる場合にはFFRの判断は通常と異なったりするのでしょうか。
塩野先生:ありがとうございます、あり得ると思います。CMDとCADが合併していた場合にFFRはCMDがなかった場合に比較して高く出ることはあります。ただ、その場合のFFRの判断としてのカットオフ値は変えなくていいと考えています。
心不全患者における微小循環障害評価の経験
宮崎要介 先生(山口大学医学部附属病院)

当院で経験した心不全患者に対する微小循環障害評価を5症例紹介する。
症例1:80歳代男性、心アミロイドーシス疑いで紹介され、精査目的で入院。心アミロイドーシスの明らかな所見はなく、LVDD 39mm、EF40%、全周性に15〜16mmの壁肥厚があり、心エコー上心アミロイドーシスを疑う所見であった。MRIでもATTR型の心アミロイドーシスが疑われ、カテーテルをしたところ有意狭窄はなかった。CFRは1.9と低下しており、IMRは67と高値であった。
症例2:70歳代男性、両手のしびれを主訴に受診、手根管症候群の診断、手術時に心アミロイドーシス疑いとなり当院に紹介。心拡大はなく肺うっ血なし。LVDD48mm、EF46%、左室壁13〜14mmと壁肥厚あり。心エコーとMRIによりATTR型の心アミロイドーシスを疑った。カテーテルをしたところ冠動脈に狭窄なく、CFRは3、IMRは24であった。
症例3:50歳代男性、心肥大で治療中にEFの低下で入院。透析治療中。LVDD58mm、EF38%、図3 全周性に11mmの壁肥厚あり。カテーテル検査で冠動脈の狭窄は認められなかった。この症例はATTR型の心アミロイドーシスは否定され、生検により心筋症とHCMと考えられた。CFRは2.1、IMRは24であった。
症例4:40歳代男性、20代で糖尿病の指摘、30代からインスリン治療、40代で透析開始。LVDD53mm、EF39%、壁肥厚は全周性に12〜13mmであった。ATTR型の心アミロイドーシスは否定的と考えれた。カテーテル検査では、LADに中等度の狭窄ありで、FFRは0.75であった。生検で心筋細胞の肥大があった為糖尿病、高血圧による心筋症と診断された。CFRは2.1、IMR9であった。IMRは低かったが、一方で、Tmn(ミ
ーントランジットタイム)が0.3と非常に速いことが確認された。
症例5:60歳代女性、呼吸困難で受診したところ心不全と診断され当院へ紹介。高血圧、頻脈性心房細動ありLVDD51mm、EF40〜45%、左室は10〜11mmと肥厚はグレーであった。左房が49mmと拡大。甲状腺機能亢進症あり。カテーテル検査では有意狭窄はなく、生検でも特異的な所見なし。CFR5.3、IMR11であった。
以上の5例の経験から4つポイントをあげる。
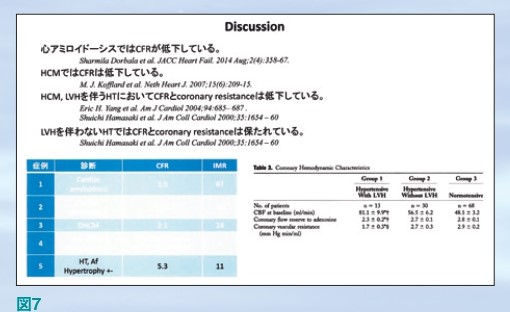
1. 心アミロイドーシス症例ではCFRが低下していることはほぼ証明されている。しかし、当院の経験から心アミロイドーシスだから必ずしもCFRが低いわけではなかった。病気の進行度合いを評価している可能性があるかもしれない。
2. HCMではCFRは低下しているということが報告されている。当院の経験とこれは一致していた。
3. HCMやLVHを伴う高血圧症例では、CFRとCoronary resistanceは低下していることが報告されている。当院の経験では、糖尿病症例でCFRが低下しているもののCoronary resistanceは上昇している症例を経験した。CFRが低下している状態ではCFRを保とうとして、ハイパーリミアを引き起こそうとしてもそれ以上血流量の増加が見込めないことが考えられた。
4. LVHを伴わない高血圧ではCFR、Coronaryresistanceは保たれている。当院の経験と一致した。
以上より、心アミロイドーシスではCFRが低下あるいは上昇しているという症例を経験したが、必ずしもそうでもないという症例も経験した。またHCMではCFR低下傾向を示していた。糖尿病歴の長い症例ではCFR、IMRともに低下していた。また、LVHは軽度の高血圧の症例では、CFR、IMRは正常の範囲であった(図7)。
園田先生:宮崎先生、ありがとうございました。室屋先生もいろいろ計測されていたと思うのですが、いかがですか。
室屋先生:心筋症などに関しては、まだら状に進行するため、心臓全体でみると宮崎先生のようになるのかなと思いました。進行度合いでしょうか。
宮崎先生:同じ患者さんで何回も測ることは難しいので詳細は分からないのですが、室屋先生がおっしゃる可能性が非常に高いと思っています。病気によってその病気の進行度や状態によって違う数値が出て
くる可能性もあると感じています。
齋藤先生:血液透析の患者さんの人口は多いと思うのですが、血液透析の患者さんの血流が特に速いと思われますか。
宮崎先生:透析患者さんでフローが速い、安静時の平均トランジットタイム自体が速い方が結構いました。一人の患者さんを連続的に見ていませんので詳細は分かりませんが、先生ご指摘のように感じています。
嵐先生:透析患者さんはとても難しいですね。検査が血液透析の前なのか後なのか、1日空きなのか2日空きなのかで全然変わります。同じ患者さんで違うタイミングで測定していくと興味深い知見が得られるように思います。


