楽天メディカルと島津製作所、米国での光免疫療法の臨床試験において1例目の被験者を登録 切除可能な原発または再発の頭頸部扁平上皮がんおよび皮膚扁平上皮がんを対象とした蛍光イメージングを用いた、ASP-1929による第Ⅱ相臨床試験
楽天メディカル社 (以下、楽天メディカル)と、(株)島津製作所(以下、島津製作所)は、蛍光イメージングシステムを用いた、ASP-1929による光免疫療法の第Ⅱ相臨床試験(治験番号:ASP-1929-103試験)において、米国国立衛生研究所の国立がん研究所で1例目の被験者を登録したことを発表した。
本試験は、「切除可能な原発または再発の頭頸部扁平上皮がんおよび皮膚扁平上皮がん」を対象とした、蛍光イメージングを用いた抗体薬物複合体ASP-1929による光免疫療法における、非盲検、単一群、Window of Opportunity(治療機会)※の第Ⅱ相臨床試験で、被験者22名を登録する予定。国立がん研究所との共同研究開発の契約に基づいて実施される本試験では、「切除可能な原発または再発の頭頸部扁平上皮がんおよび皮膚扁平上皮がん」を対象に、標準治療の外科的腫瘍切除前に、ASP-1929を用いた光免疫療法による単回治療を実施した場合の有効性および安全性を評価する。さらに、島津製作所の蛍光イメージングシステムを用いて、ASP-1929に含まれる光感受性物質IRDye® 700DX(以下、IR700)の蛍光発光を、リアルタイムに観察・記録し、臨床における利用可能性を評価する。
楽天メディカルのチーフ・エグゼクティブ・オフィサーである三木谷浩史氏は次のように述べている。「当社は、ASP-1929を用いた光免疫療法単独の治療や抗PD-1抗体との併用治療にて、切除不能な再発頭頸部扁平上皮がんおよび皮膚扁平上皮がんを対象とした試験を実施しています。今回の試験では、患者群を拡大して、手術で切除可能なこれらの原発がんを対象としています。本試験の結果によって、一人でも多くの患者さんに、楽天メディカルの光免疫療法をお届けできることに繋がればと願っています。」
島津製作所の代表取締役社長である上田輝久氏は次のように述べている。「光免疫療法の為、当社の蛍光可視化技術を用い、楽天メディカルと蛍光イメージングシステムを開発しました。今回、本試験では、腫瘍部の状態の可視化を行うため、当社の技術による蛍光イメージングシステムで光免疫療法の光照射中のIR700の反応をリアルタイムに観察・記録します。早期がんを含む多くの患者さんに、一日も早く本治療をお届けすることに、当社の蛍光可視化技術が貢献できることを願っています。」
ASP-1929を用いたその他の試験については、楽天メディカルが、再発頭頸部扁平上皮がんを対象とした国際共同第Ⅲ相臨床試験、および、米国にて頭頸部扁平上皮がんおよび皮膚扁平上皮がんを対象とした抗PD-1抗体との併用療法による第Ⅰb /Ⅱ相臨床試験を実施している。また、2020年9月に、日本において、ASP-1929およびレーザ装置は、「切除不能な局所進行又は局所再発の頭頸部癌」を適応として厚生労働省より製造販売承認を取得した。
※Window of Opportunity Study(治療機会)試験は、被験者ががんと診断されてから標準治療が開始されるまでの短期間に、非標準的な治療、または被験者にとって重要性のある治療を実施するもの1)2)。
1)Aroldi F, Lord SR. Window of opportunity clinical trial designs to study cancer metabolism. Br J Cancer. 2020;122(1):45-51. doi:10.1038/s41416-019-0621-4
2)Schmitz S, Duhoux F, Machiels JP. Window of opportunity studies: Do they fulfil our expectations? Cancer Treat Rev. 2016 Feb;43:50-7. doi: 10.1016/j.ctrv.2015.12.005. Epub 2015 Dec 31. PMID: 26827692.
ASP-1929について
楽天メディカル社は、2013年以来、独占的ライセンスを有する光免疫療法により開発された技術基盤であるイルミノックス®プラットフォームを基に、新たながん治療を開発している。イルミノックス®プラットフォームを基に開発された最初の開発品であるセツキシマブ サロタロカンナトリウム(開発コード:ASP-1929)は、抗体であるセツキシマブに光感受性物質のIRDye® 700DX が結合した抗体薬物複合体。頭頸部がん、食道がん、肺がん、結腸がん、すい臓がんなど様々な種類の固形がんに発現する上皮成長因子受容体(EGFR)に結合する。がん細胞と結合後、レーザ光(690 nm)を専用のレーザ照射システムを用いて照射することにより局所的に励起される。本医薬品は、厚生労働省から先駆け審査指定制度の対象品目として指定され、条件付き早期承認制度の適用のもと申請を行った。また米国食品医薬品局からファストトラックに指定され、現在再発頭頸部がんの国際第Ⅲ相臨床試験を実施している。日本において、切除不能な局所進行又は局所再発の頭頸部癌を適応とし厚生労働省から承認を受けている。日本以外の規制当局による承認は受けていない。
イルミノックス®プラットフォームについて
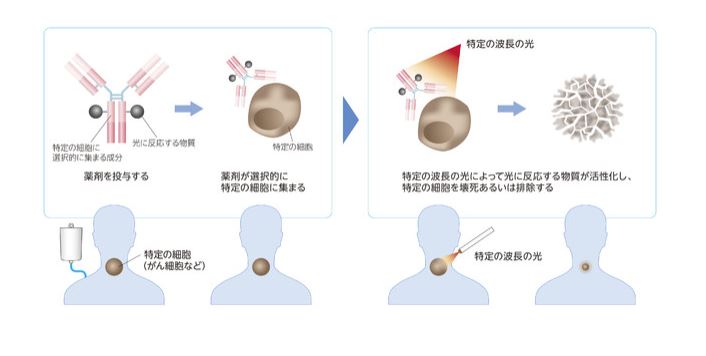
イルミノックス®プラットフォームは、治療技術基盤の名称であり、米国国立がん研究所の小林久隆氏らが開発したがん光免疫療法が基となっている。同プラットフォームは、医薬品、医療機器、医療技術、その他周辺技術を総合的に利用した技術基盤であり、楽天メディカル社は、これに基づき製品や治療法の開発を進めている。イルミノックス®プラットフォームとは、薬剤と光を組み合わせた、がんをはじめとした様々な疾患に対する新しい治療法を開発するための技術基盤。同プラットフォームを用いた治療は、「薬剤の投与」と「光の照射」の 2段階で構成される。薬剤は、光感受性物質 (光に反応する物質) と、キャリア (特定の細胞に選択的に集積する成分) から組成される複合体。同薬剤を投与し、特定の細胞に選択的に集積した後、その細胞に特定の光を照射することで光感受性物質が活性化し、生化学・物理学的プロセスにより、特定の細胞を壊死、あるいは、排除する。
楽天メディカル社について
楽天メディカル社は、イルミノックス®プラットフォームと呼ぶ技術基盤を基に、薬剤と光を組み合わせた、がんをはじめとした様々な疾患に対する新しい治療法の開発を行うグローバルバイオテクノロジー企業である。同プラットフォームを基に開発された医薬品・医療機器の前臨床試験では、特定の細胞の速やか、かつ選択的な壊死をもたらすデータが示されている。楽天メディカル社は、がんを克服するというミッションを掲げ、がん患者さんがより良い生活を送れる社会の実現を目指している。米国に本社と研究開発拠点を構え、日本、オランダ、台湾、スイスの世界5 カ国を拠点としている。楽天メディカル株式会社は、米国法人である楽天メディカル社の日本法人。
楽天メディカル
https://rakuten-med.com/jp/ https://rakuten-med.com/jp/
島津製作所について
株式会社島津製作所は、社是「科学技術で社会に貢献する」、経営理念「人と地球の健康への願いを実現する」のもと、分析計測機器、医用機器、航空機器、産業機器などの事業を展開している。当社は、光免疫療法の計測技術の開発を進めるため、米国国立がん研究所と共同研究開発の契約、および国立がん研究センター東病院と共同開発の契約を締結した。
(株)島津製作所
https://www.shimadzu.co.jp/