GEヘルスケア・ジャパン、PET検査用薬剤合成装置「FASTlab」「FASTlab2」におけるアミロイドPETイメージング剤「ビザミル(TM)」の効能効果追加に係る製造販売承認事項一部変更承認を取得
~アルツハイマー型認知症診断・治療薬開発治験へのさらなる貢献を目指す~
医療の課題解決に取り組むGEヘルスケア・ジャパン株式会社(本社:東京都日野市、代表取締役社長兼CEO:若林 正基)は、PET(陽電子放射断層撮影装置)検査で使用する放射性薬剤を自動合成する放射性医薬品合成設備「FASTlab(ファストラボ)」および「FASTlab2(ファストラボツー)」におけるアミロイドPETイメージング剤「ビザミル(TM)(VIZAMYLTM、一般名:フルテメタモル)、以下”ビザミル”」について、10月30日付けで「アルツハイマー病による軽度認知障害又は認知症が疑われる患者の脳内アミロイドベータプラークの可視化」の効能又は効果に係る国内承認事項一部変更承認を取得した。
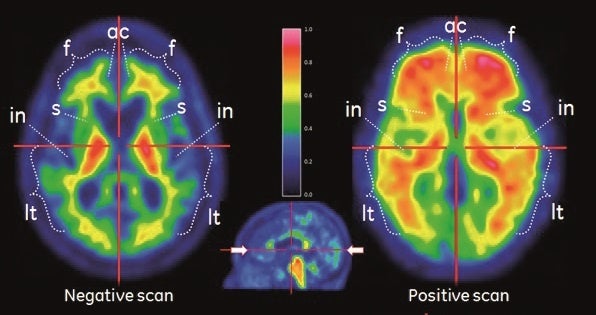
アミロイドβ 陰性画像(negative scan)と陽性画像(positive scan)
先日、アルツハイマー病による軽度認知障害および軽度の認知症の進行抑制を効能効果とする新たな治療薬(疾患修飾薬)の製造販売承認が発表されたが、この治療薬の使用には承認を受けた診断法によりアミロイドβ病理を示唆する所見を確認することが求められる。ビザミルは、アルツハイマー病による軽度認知障害又は認知症が疑われる患者の脳内アミロイドベータプラークを可視化するPET用薬剤である。このことから、ビザミルによるアミロイドPET検査は、非侵襲的に脳内のアミロイドβの沈着を評価できる検査方法として大きな期待と注目が寄せれれている。
GEヘルスケア・ジャパンは、2015年にPET検査用薬剤合成装置「FASTlab」での「ビザミル(TM)」合成機能の薬事承認を取得した。そしてこの度、アルツハイマー病による軽度認知障害又は認知症が疑われる患者の脳内アミロイドベータプラークの可視化について本剤の対象とすべく、本年5月に「FASTlab」および「FASTlab2」の承認事項一部変更承認申請を行い10月30日付けで承認を取得した。今後「FASTlab」および「FASTlab2」ビザミルの合成用カセット(フルテメタモル合成用カセット)がアミロイドPET検査に活用され、アルツハイマー病の早期診断や適切な治療へ貢献できることを期待している。

放射性医薬品合成設備FASTlab2
PET薬剤合成用の放射性医薬品合成設備「FASTlab」は、2015年に国内で初めて1台で複数のPET用薬剤(FDGおよびビザミル)が合成可能な装置として承認を取得した。院内合成を実施する施設における限られたスペースおよび時間内で1日に2剤の合成が可能であることは、疾病診断にPET装置を活用しサイクロトロンによる院内合成を実施する施設において、設備投資やワークフローの面で効率的で有用なインフラとなる。
超高齢社会を迎えた日本では、2025年には国内の認知症患者数が700万人を超え、約5人に1人が認知症高齢者になるとの推計がされている。この大きな社会問題の中で、アルツハイマー病による軽度認知障害および軽度の認知症の進行抑制を効能効果とする新たな治療薬が製造販売承認を受けたことは大変素晴らしいニュースであり、その適正使用のためにアミロイドPET検査が大きな役割を果たすと期待している。現在、国内でPET・PET/CT装置を保有されているご施設約400施設のうち、サイクロトロンを保有しPET放射性薬剤の院内合成を行っているご施設は約150施設あり、主にFDGによるがんのPET検査が実施されている。今後これらのご施設において「FASTlab」「FASTlab2」およびビザミルの合成用カセット(フルテメタモル合成用カセット)が、認知症の早期診断や早期治療に大きく貢献できることを期待している。
本件に関するお問い合わせ
GE ヘルスケア・ジャパン(株)
コーポレート コミュニケーション
TEL: 0120-202-021

