第52回日本胆道学会学術集会ランチョンセミナー6
肝門部領域胆管癌に対する術前診断と胆道ドレナージ
日時:2016年9月30日
場所:新横浜プリンスホテル
共催:東芝メディカルシステムズ株式会社
司会
手稲渓仁会病院消化器病センター
真口宏介先生
講演1 外科の立場から
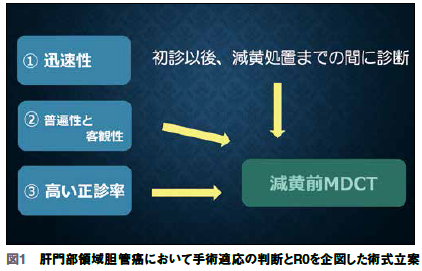
外科医の立場から見た肝門部領域胆管癌における術前診断の最も重要な目的は「手術適応の判断とR0(癌の遺残なし)を企図した術式立案」をすることであり、このために診断法には迅速性、客観性と普遍性、高い正診率が求められる。当院ではこれまでMDCTを基軸として術前診断を行っているが、204例切除のうちR0切除率は89%であり、良い診断率ではないかと考えている。MDCTを基軸として術前診断について症例をまじえ、解説する。
KEY SENTENCE
●減黄前にMDCTを撮影することがガイドラインでも勧められており、MDCTを基軸とした術前診断が重要である。
●3次元立体解剖を考える上で注意すべき点は胆管のアノマリーだけでなく、肝動脈のアノマリーも挙げられる。
●MDCTの診断が大変重要ではあるが、外科や内科間で密な連絡を常に取れる体制が大切。
R0を導く手術立案のためのMDCT診断
肝門部領域胆管癌の外科治療の成功は「術前診断と術前管理に5割」「手術に4割」「術後管理に1割」にかかっていると考えている。特に、術前の診断が治療結果に直接影響することもあり、正確な診断が重要。外科医の立場から見た肝門部領域胆管癌における術前診断の最も重要な目的は「手術適応の判断とR0(癌の遺残なし)を企図した術式立案」であり、診断法には①迅速性、②客観性と普遍性、③高い正診率が求められる。①の迅速性に関しては初診から減黄処置までの時間をなるべく短くする必要がある。現在、減黄方法はENBD(Endoscopic Nasobiliary Drainage:内視鏡的経鼻胆道ドレナージ)が主流であるが、ENBDを予定残肝領域に入れるためにはENBD挿入前に術式が決められていないといけない。当院では患者が初診で来られたその日にCTを撮影して診断を行い、翌日にはENBDを施行している。普遍性と客観性に関してはCT画像が有効である。例えば超音波内視鏡は施行した医師や術者の解説がなければ解剖や診断の理解は難しいが、CTは解剖の理解に解説は必須ではない。さらに結果として選択した術式が正しくR0を導くものでなければならないため、③の高い正診率が必要となってくる。現在は減黄前にMDCTの撮影がガイドラインでも勧められている(図1)。当院ではこれまでMDCTを基軸として術前診断を行っており、204切除例のうちR0切除率は89%であり、良い診断率ではないかと考えている。
●症例1
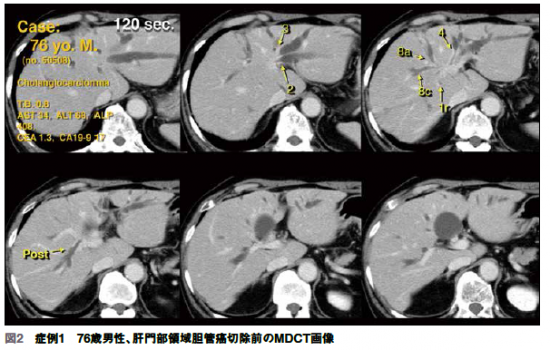
当院は2002年に開院し、16列CTが開院と同時に導入された。当院の第2例目の肝門部領域胆管癌の切除例を紹介する。76歳男性で総ビリルビン値が0.8の肝機能障害で当院に紹介され、当時は黄疸が出ず腫瘍マーカも正常値であった。CT画像より、肝内胆管の末梢は拡張しているが肝門部に近づくに従って細くなっていることがわかる(図2)。下流側では膵内まで胆管壁の肥厚と造影効果が見られる。今であれば胆管癌だと気がつくが、MDCTが発売された当初はそれまでヘリカルCTの画像に見慣れており、MDCTで撮影した画像を経験したことがなかった。「黄疸もないし胆管癌なのだろうか?」と悩んだことを記憶している。PTBD(Percutaneous Transhepatic Biliary Drainage:経皮経肝的胆道ドレナージ)を施行し、胆汁細胞診をしたところ腺癌の所見であり、やはり胆管癌であった。当院において、MDCTで胆管癌の所見が確認できた初めての症例である。切除可能かを考えると、後区域も前区域もS4も残存させるのは難しく、唯一、外側区域動脈枝のすぐ右側で胆管を切る肝右3区域・尾状葉切除、膵頭十二指腸切除、門脈合併切除再建を行えば良いと、このCT画像を見ながら考えた。実際に、切除標本と比較しても胆管壁の肥厚や内腔の様子などが術前のCT画像とよく似ていた。「CTを見るだけで術式まで決めることができる」ということに気がついた症例であった。
それまでは肝門部領域胆管癌の診断は多くのモダリティを要し、複雑であった。PTBD、PTCS(Percutaneous Transhepatic Cholangioscopy:経皮経肝胆道鏡)、門脈造影、血管造影など侵襲的な検査も多く、時間もかかっていた。しかしながら前述の症例を経験して、MDCTは胆管内腔の変化や壁の性状を同時に確認でき、血管との関係も理解しやすいという点に気がついた。さらにその後、術式を決定するためにはMDCTを減黄前に撮影する必要があるとわかり、検討を重ねてきた。
MDCTによる肝門部3次元解剖の把握と進展度診断の重要性
肝門部領域胆管癌の術前診断・管理体系におけるMDCTの位置付けについて述べる。当院では肝門部領域胆管癌が疑われたら、その日のうちにMDCTを撮影し、進展度診断と手術適応の判断と術式立案を行っている。さらに3D angiographyも撮影している。以前はPTBDだったが、現在はENBDを予定残肝領域にのみ経乳頭的に入れている。そこから胆道造影を行い、同時にマッピング生検、適応があればIDUS(管腔内超音波検査法)やPOCS(経口胆道鏡)を行う。予定残肝機能をICGとCTvolumetryで評価し、必要に応じて門脈枝塞栓術を施行し、手術に向かうという、MDCTを基軸とした術前診断体系を実現している(図3)。
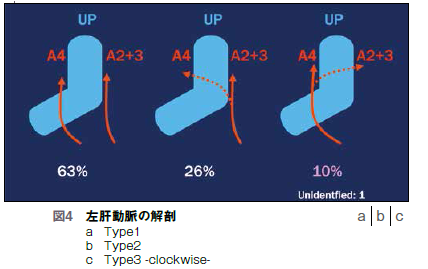
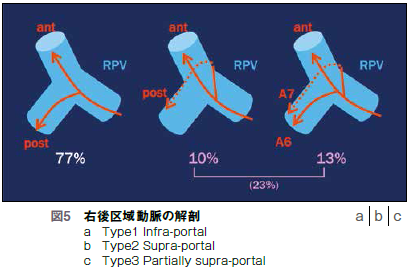
水平方向と垂直方向で進展度診断を行い、かつ胆管、動脈、門脈のアノマリー(通常の解剖構造と異なること)やその3次元立体解剖を十分に理解して術式を決める。水平方向進展度診断は胆管壁の性状と内腔系の変化の両方に着目し、垂直方向進展度診断では主に門脈や動脈と腫瘍の間の脂肪層の有無に着目する。3次元立体解剖を考える上では胆管のアノマリーの他に肝動脈のアノマリーも重要である。左系においてはA4と外側区域の動脈の出方は様々で、Type1(図4a)はA2+3がUP(門脈臍部)の左、A4がUPの右を通るタイプで最も多いが、左側からA4がUPの裏を通る(図4b)、または、少ないアノマリーだがUPの右側から外側区域の動脈が出るものもある(図4c)。Type3は右3区域の切除時には特に注意が必要である。右系においては後区域動脈が通常Infraportalであるのに対し、完全にSupra-portal、あるいは部分的にSupra-portalになっているものが約20%存在する(図5)。このような場合、左葉切除あるいは左3区域切除を行う際には注意が必要になるため、これを術前に十分把握する。
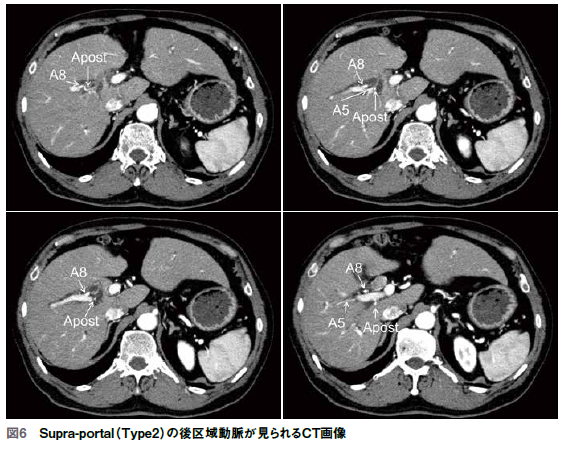
例えば図6の症例はSupra-portal( Type2)の後区域動脈があり、axial画像で見るとA8からSupraportalの動脈が走行している。さらに尾側を観察すると右門脈が現れて、Supra-portalの動脈が胆管にそって後方にある。
術式を立案するためには、どこで胆管が切除できるかを考えなければならない。右肝切除ではUPの右縁がメルクマールで、右3区域切除ではUPの左縁がメルクマールである。そして左葉切除ではカントリー線と前区域の胆管が交差するライン、後区域側では右門脈の前縁くらいまでに癌浸潤がおさまっていることをメルクマールにする。しかし実際には中肝静脈の背側へ肝を切り込むと、さらに奥まで前区域も切除できる。後区域はあまり深く切除すると再建できなくなるため、右門脈のやや背側で切除することを想定しなければいけない。左3区域切除では右門脈の後縁までに癌が浸潤していないということが重要であり、これを事前にCTのaxialとcoronalで把握し、それに基づいて術式を考えなければならない。
●症例2
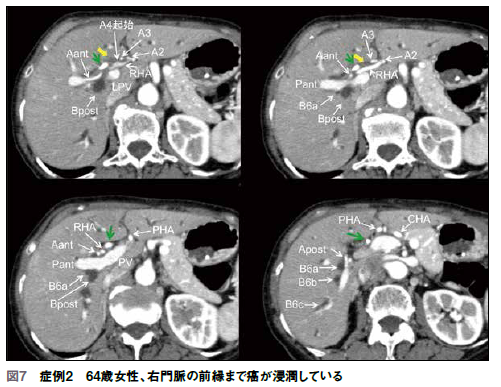
64歳女性の症例、前医で右前枝にENBDが留置され、来院時には総ビリルビン値は1.3であった。CTでは、左葉系の動脈(A2、A3、A4)および左門脈は癌浸潤を受けている。右肝動脈も癌浸潤を受けており、これが前・後分岐部におよんでいる。胆管後枝側への浸潤は、右門脈前縁より深いところまでおよんでいる。以上から、この症例では、左3区域・尾状葉切除、門脈・右肝動脈合併切除・再建以外では根治させる術式がないことがわかる(図7)。このためB6からPTBDを追加することにした。CTを正しく判断していればはじめから後区域だけに胆道ドレナージを入れれば良かったが、このようなことが実際にはしばしば経験される。これはCTをきちんと読影すればわかることである。
●症例3
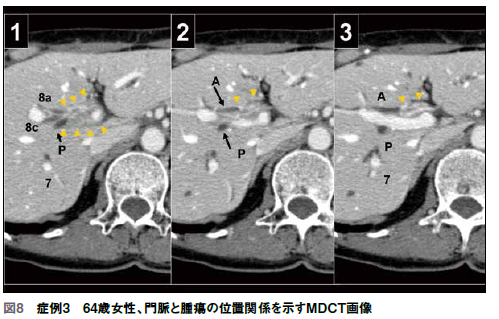
もう一例を示す。64歳女性、無黄疸で総ビリルビン値は0.9。CTでは肝門部に腫瘍がある。門脈系を見ると、左門脈はその根部からUP起始部まで癌にまきこまれている。右肝動脈も浸潤を受けている。後区域胆
管側への腫瘍の浸潤は、右門脈後縁レベル近くにまで達している(図8)。以上から、術式は、左3区域・尾状葉切除、門脈・右肝動脈合併切除再建しかない。この術式を想定してCT Volumetryを行ったところ、残肝K値は0.052だったため、門脈塞栓術やドレナージをせずに切除した。病理では、腫瘍は尾状葉や門脈にも浸潤しており、右肝動脈の周囲のごく近くまで癌浸潤があったが、この方は術後10年も癌の再発がない。
このようにMDCTを丹念に読影することで術式を決定できる。しかし限界もある。よくいわれるように表層拡大進展はCTでは判別がつかないことが多い。良性胆管狭窄もはっきりと区別は難しい。また前医で減黄処置がなされると正確な診断は不可能である。
●症例4
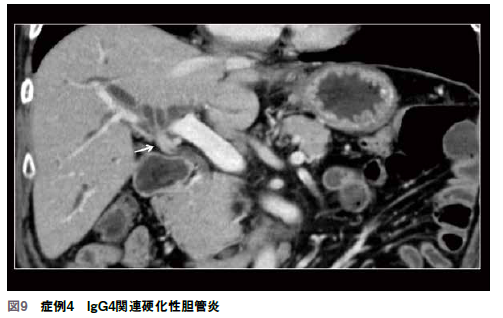
この例はIgG4関連の硬化性胆管炎であり胆管壁が肥厚している(図9)。見慣れた現在であればこれは硬化性胆管炎かもしれないと予見できるが、このときは胆管癌だと判断して、胆管生検はネガティブであったが切除を施行した。すると壁の肥厚は確かに存在したが粘膜はきれいで、IgG4関連硬化性胆管炎であった。やはりCTでは明瞭にこの領域を区別できないことが多い。
最後に
肝門部領域胆管癌に対して根治切除ができるかどうか判断するためには、MDCTの診断が大変重要ではあるが、前提として、肝門部領域の解剖と手術の内容の両方を知っている必要がある。そのためには手術のポイントや手技を熟知した胆道外科医が必要である。経験豊富な胆道外科医が読影しなければ正しい判断は不可能である。患者さんが外科と内科、どちらに来院しても、お互いに連絡を密に取り合うことが必要である。当院では患者さんが内科を受診すれば「先生、この症例は切除できますか?」と外科に必ず相談が来る。また外科に来れば「ENBDを挿入してください」と内科に連絡する。このような密な連絡を常に取れる体制が重要だと考える。
講演2 内科の立場から
肝門部領域胆管癌に対する術前診断とドレナージについて内科の立場から述べる。CT所見から進展範囲を診断し、想定術式を決定後、生検すべき部位・ドレナージ枝を決めてERCPを施行する。実臨床では生検によっても質的診断が困難である症例も多いのが現状である。また、肝門部領域胆管癌はドレナージ後もドレナージできない枝が残ることが多く注意が必要である。術前診断とドレナージの実際について当院の症例を供覧し解説する。
KEY SENTENCE
●肝門部領域胆管癌では、ドレナージできない領域が存在するため、造影時に注意を要する。
●炎症や黄疸がある場合、生検をしても診断が難しく、病理診断に偽陽性や偽陰性があることを認識する必要がある。
●肝門部領域胆管癌ではドレナージ後の逆行性感染の防止が重要である。
●術前の胆管炎を防ぐためにENBDが最良の選択とされるが、患者にとっての苦痛は大きく、さらなる改善が必要である。
肝門部領域胆管癌の診断の実際
内科の立場から肝門部領域胆管癌の診断とドレナージについて述べる。まずはCTを読影し、進展範囲を診断し想定術式を考慮して生検すべき部位、ドレナージ枝を判断する。
●症例1
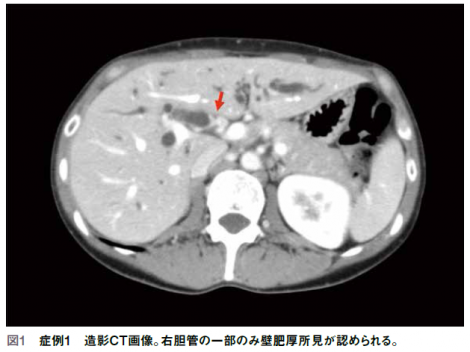
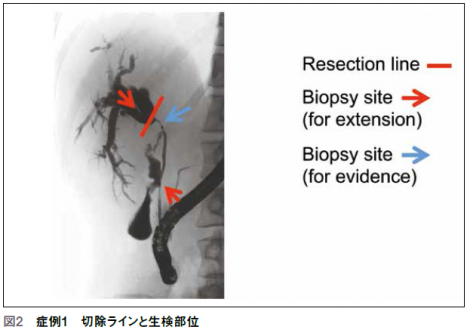
この症例では肝門部に壁肥厚が認められたが右胆管には軽度進展しているのみであり(図1 赤矢印)、想定術式はL2+S1であると判断した。この場合、予定残肝となる右葉をドレナージすべきである。左3区域切除ではなく、左2区域切除で十分であるということを確認する目的で生検する場所は前枝と後枝の合流部となる。次にE R C P (Endoscopic Retrograde Cholangiopancreatography:内視鏡的逆行性胆管膵管造影)でCTの所見を確認する。肝門部領域胆管癌はドレナージされない領域が残ることがあるため、このような領域をあまり造影しないよう注意すべきである。この症例ERC(Endoscopic Retrograde Cholangiography: 内視鏡的逆行性胆道造影) とIDUS(Intraductal Ultrasonography:管腔内超音波検査)所見では前枝と後枝の分岐部には壁肥厚は認められず進展なし、狭窄部では壁肥厚が認められ、RHAと接しているが浸潤はないであろうということが確認できた。続いてIDUS で分からないような進展の有無を調べるためにIDUSでは進展がないと考えられる部位を進展範囲診断目的に生検する。この際、想定術式が左2区域では前枝後枝の合流部と膵上縁を生検し、右2区域の場合はB4の合流部を生検する。左3区域切除の場合は後枝の頂部を生検し、右3区域切除の場合はB2とB3の合流部を生検する。この症例の場合は悪性腫瘍のエビデンス目的で青矢印部分を生検し、下の赤矢印は膵上縁部の生検となる(図2)。腫瘍部位からの生検はコンタミを防止する目的で可能な限り最後に行う。以前は一回に一度の鉗子の開け閉じで組織採取を終了していたが、最近は一回の採取時に三回ほど鉗子を開け閉じしている。これにより大きく組織が採取できる。最後にENDO(Endoscopic Nasobiliary Drainage:内視鏡的経鼻胆道ドレナージ)を予定残肝枝に挿入し、吸引が良好であることを透視下で確認して終了する。この症例の生検結果は胆管狭窄部でadenocarcinoma、前枝後枝の合流部及び膵上縁では進展は認められず、L2+S1の手術が施行された。
診断方法の工夫と診断の難しさ
当科ではCTとERC、IDUS、経乳頭的胆管生検で進展範囲診断と質的診断を行っている。IDUSのメリットはESTなどを負荷しなくても容易に進展範囲診断が可能な点である。しかし、上皮を置換するような表層進展はIDUSでは診断困難であり生検が必要となる。生検鉗子はガイドワイヤの脇から挿入するので目的部位に挿入困難であることもある。そのための工夫として8.5Fr Through-Pass(Gadelius Medical) の外套のみを使用して生検をする方法が報告されている。上流側に一回ガイドワイヤが入れば、鉗子の目的胆管枝への挿入が容易になるため臨床的に有用性が高い方法だと考えられる。またもう一つの工夫にTrefle(Piolax Medical)がある。これはEST( 内視鏡的乳頭切開術: Endoscopic Sphincterotomy) をしなくても施行可能であり、狭窄部の生検が容易となるが進展範囲診断は不能で組織採取後の処理がやや煩雑である。
●症例2
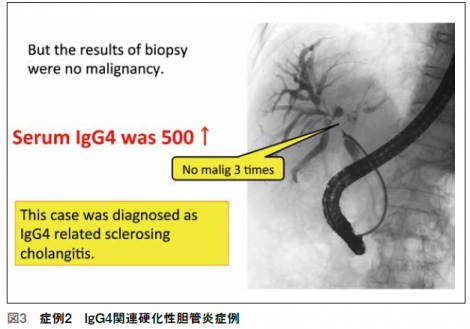
ここからは診断困難例を供覧する。この症例も肝門部領域胆管癌疑いにて当院に紹介された(図3)。前医でESTがなされていたため胆道鏡を施行したところ、胆道内部に明らかな腫瘍と見られる所見が得られた。しかしながら生検を行っても悪性診断は得られず、IgG4を測定すると高値であったためIgG4関連硬化性胆管炎と診断し、ステロイドを投与したところ3ヶ月後には狭窄が改善していた。胆管生検にて癌だと確診できる症例は当院でも7割程度であり、特に炎症や黄疸があると診断が難しいことが多い。病理診断に偽陰性・偽陽性があることを認識する必要がある。
●症例3
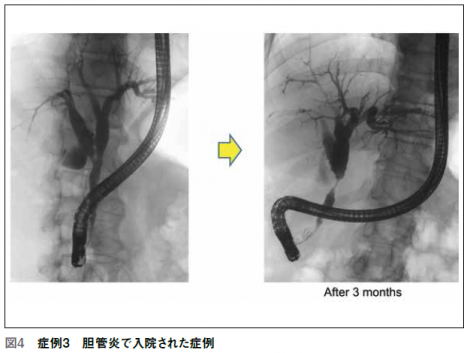
胆管炎で当科の関連病院に入院、下部胆管の不整が気になるということで紹介された。生検するとAtypicalcells(良性異型細胞)の結果のみでありフォローアップすると下部胆管の不整所見は改善しているように見えた。しかし、生検を行うと一部でadenocarcinomaと診断された。このため胆道鏡を施行するも明らかな悪性所見は得られず、再度生検を行うもAtypical cellsが見られるのみであった。良性か悪性か判断しかねるため、手術か経過観察か悩んだが、胆管癌であれば進行は早くないだろうと考え3ヶ月間経過観察を行うことにした。しかし、3ヶ月後には狭窄が進展しており(図4)、生検を行うと様々な箇所でadenocarcinomaと診断され、手術不能となってしまった。生検の診断能は当院では感度76.5%、特異度100%という結果が得られている。癌組織が生検で得られれば癌の診断は容易である。しかし、良性病変を良性と診断するのは困難なことがある。数多く採取すれば成績は向上するため、質的診断を行う場合、特に良性狭窄を疑う症例の場合、最低3個の生検が必要であると考える。また組織がしっかり採取できても癌と診断困難な場合(偽陰性例)もある。当科の検討では、生検の結果が偽陰性であった症例でIMP3という免疫染色を実施した結果、19例中12例が陽性であった。逆に最終診断癌陰性であった12例のうち1例のみが陽性であった。実際の臨床では免疫染色することは少ないが、IMP3免疫染色陽性を癌と診断することにより診断率向上に寄与する可能性があると考えている。
どのようにドレナージするか
肝門部領域胆管癌の術前ドレナージは、予定残肝枝のみのドレナージであるためドレナージ後もドレナージされない枝が残る。このためドレナージ後の逆行性感染を防ぐことが最も重要だと考えている。一方、2013年に欧州から「肝門部領域胆管癌術前のドレナージは不要」という論文が発表されている1)。この論文では多くの症例で術前ドレナージにEBS(Endoscopic Biliary Stenting:内視鏡的胆管ステンティング)が行われており、胆道感染のMorbidity rateが32.7%で少し高い印象を受ける。確かにMortality rateは10%前後で術前にドレナージした例としていない例で差はないが、右葉切除時のMortality rateは22%と非常に高くなっていることが問題である。日本の場合は名古屋大学、北海道大学、東北大学、千葉大学からの報告におけるMortality rateは2~8%と欧州にくらべ良好であり、術前の我々のドレナージがMortality rateに寄与しているのではないかと考えている2)。日本では術前胆道ドレナージが必要とされ胆道癌診療ガイドライン20153)でもエビデンスレベルCで推奨されている。胆道ドレナージには外瘻のPTBD、ENBDと内瘻のEBSがあるが術前の胆管炎を防ぐために、外瘻でのアプローチが日本では常識的であり推奨されている(図5)。現在ではENBDの選択が最も良いとされるが、この手技は患者にとって苦痛が大きいため、さらなる改善が必要であろうと考える。
●症例4
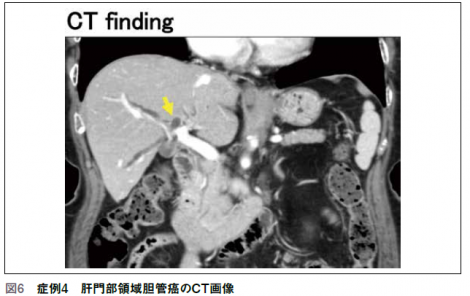
ENBDの症例を呈示する。肝門部領域胆管癌の例でRHAに浸潤が認められ、後区域枝までの進展はないためL3+S1+RHAが想定術式であった症例である(図6)。
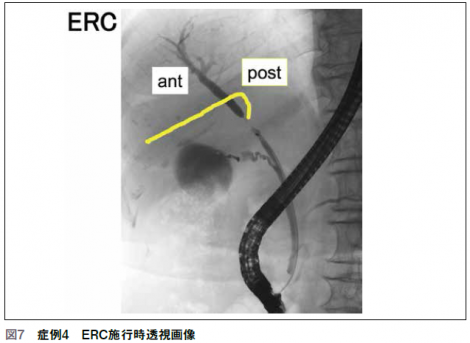
ERCを施行すると前枝は確認できるが、後枝が造影されなかった(図7)。これに対してガイドワイヤを使用して後枝を選択、前枝の造影剤を吸引して後枝で造影した。このあと生検を行い、ENBDを挿入した。ENBDのカテーテルは以前360° 屈曲したカテーテルを使用していたが、現在は屈曲が270°程度で側孔が多いものを使用している。
当院におけるENBDの実績とリスクファクター
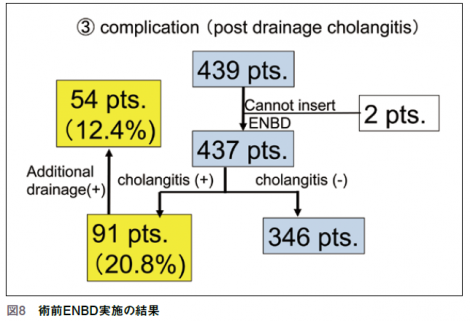
当院では肝門部領域胆管癌術前のENBDを439例施行しており、予定残肝枝に挿入可能であったのは410例(93.4%)、挿入不能であった例が28例、そのうちPTBDが21例に施行されていた。黄疸を有する症例のみで検討するとENBD挿入前の「総ビリルビン値高値」「胆管炎の存在」がENBDによる減黄効果が悪いリスクファクターであった。ENBD施行後に胆管炎を発症したのが410例中91例(20.8 %) で、そのうちの54例(12.4%)に追加のドレナージが施行された。ENBD挿入後の胆管炎へのリスクファクターは「ESTの施行」と、「ENBD術前に胆管炎あり」の2点であった。膵炎は439例中67例(15.2%)で起こっており、リスクファクターは「膵管造影」あるいは「前もってEBSやENBDが挿入されていないこと」であった。最終的には439例中315例(71.8%)が膵炎や胆管炎、チューブトラブルを起こすことなく経過していた(図8)。
おわりに
肝門部領域胆管癌の診断、ドレナージは奥が深い。まだまだ進歩の余地が残されている領域である。特に手術前は外科医と内視鏡医が緊密に連携し、安全かつ積極的な手術に役に立つ手技のみ施行することが重要である。
<文献>
1) Farges O et al: Multicentre European study of preoperative biliary drainage for hilar cholangiocarcinoma. Br J Surg 100(2) :274-83,2013
2) Nagino Masato:Perihilar cholangiocarcinoma : a surgeon’s viewpoint on current topics. Journal of
gastroenterology 47(11):1165-1176, 2012
3) 日本肝胆膵外科学会ほか:胆道癌診療ガイドライン第2版. 医学図書出版,2014